|
|
| Proprietates generales
|
| Nomen, Symbolus, Numerus Atomicus
|
magnesium, Mg, 12
|
| Proprietas generalae
|
| Nomen, Symbolus, Numerus atomicus
|
Magnesium, Mg, XII
|
| Turma, Periodus, Glaeba
|
II, III , s
|
| Color
|
album, argenteus 
|
| Pondus atomicum
|
24,3050(6) uam
|
| e-
|
2, 8, 2
|
| Proprietas physicae
|
| Status
|
Solidus
|
| Densitas
|
1738 kg/m3
|
| Densitas ad punctum liquofactu
|
1584 kg/m3
|
| Punctum liquofactu
|
923 K (650 °C)
|
| Punctum fervoris
|
1363 K (1090 °C)
|
| Proprietas atomicae
|
| Structura crystallina
|
Cubica
|
| Radius atomicus
|
150 pm
|
| Radius atomicus (calc.)
|
145 pm
|
| Radius covalenta
|
130 pm
|
| Radius van der Waals
|
173 pm
|
| Varietas
|
| Duritas Mohs
|
2,5
|
| Duritas Brinell
|
260 MPa
|
| Isotopa stabila
|
|
|
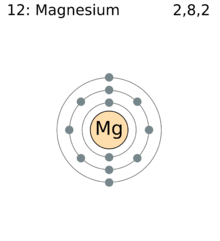 Configuratio electronica magnesii: nucleus, et electrones duodecim.
Configuratio electronica magnesii: nucleus, et electrones duodecim.
Magnesium[1] (-ii, n.) est elementum chemicum metallicum alcalicum terrenum cui symbolus Mg et numerus atomicus duodecim sunt. Magnesium est octavum elementum et tertium metallum, pone aluminium et ferrum, de eis quae solidam terrestrem crustam componunt. Magnesium circa duas centesimas ponderis crustae facit. Magnesium est tertium inter elementa chemica quae in aqua marina diluta sunt.
- ↑ "Magnesium": Peter van der Krogt, "Elementa chemica" apud situm Elementymology & Elements Multidict
Nexus interni
Elementa chemica: series paginarum brevium




